GMP飞检重点企业的类型
1、产品被药监局抽检不合格的企业。
2、被监管部门发放告诫信的企业。
3、注册现场检查或GMP认证检查被发现存在缺陷较多的企业。
4、国外检查机构被发现存在较严重缺陷的企业。
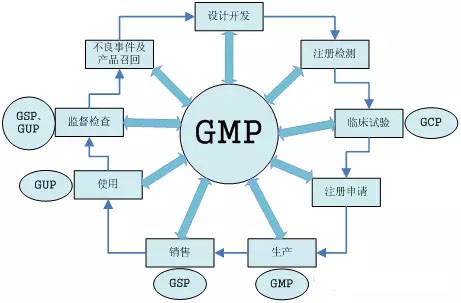
飞行检查的范围
1、检查的范围:医疗器械研制、生产、经营和使用的全过程。
2、检查的对象:
(1)经投诉举报或者其他来源的线索表明可能存在质量风险的企业(对于高风险程度产品,必将成为检查的重点);
(2)被检验发现存在质量风险的企业(如:省级以上单位的监督抽查);
(3)医疗器械不良事件监测提示可能存在质量风险的企业;
(4)被发现申报资料存在真实性疑问的企业(如:注册申报、生产许可等);
(5)涉嫌严重违反质量管理规范要求的企业(违反质量管理规范被监管单位发现的);
(6)有严重不守信记录的企业(部分省市已建立了诚信档案,有不良记录的,将是飞检的重点);
(7)其他需要开展飞行检查的情形。
飞行检查的类型
1、检查人员组成:通常由2名以上检查人员组成,检查组实行组长负责制,并由当地药监部门派出相关领域专家参加检查工作。
2、检查形式:突击检查,受检单位及检查内容及时间保密、检查进展保密、采集证据迅速、直接。
3、检查方式:企业相关场所无条件向检查组开放,核对企业现场实物,确认产品质量,直接现场调查取证并记录,必要时抽样送检验部门;对存在疑问或异常的货物进行封存。
如何应对飞检
从近两年飞检的通报来看,企业出现问题主要体现在以下8个方面。
1、人员培训不到位:未对关键及特殊岗位进行相应的培训。
2、生产管理不到位:未制定受控的关键和特殊过程的作业指导书;未对关键和特殊过程的重要参数进行验证或确认。
3、质量控制不到位:检验方法及判定规则不明确、出厂检验未按要求进行、现场未做检验标识。
4、未对质量管理体系的运行进行评价和审核:未按要求进行内审、定期召开管理评审。
5、厂房设施不满足生产条件:仓库贮存条件及设施不符合要求,生产工艺不完善,生产条件不符合要求。
6、设计开发管理不到位:未建立全套完整的设计开发文档,未保持设计更改记录。
7、质量体系文件管控不到位:检验规程与产品技术要求规定不一致、未制订放行程序、未按检验方法检验。
8、不合格品控制不到位:不合格品未按要求进行标识、记录、隔离、评审。